Anvisa aprova medida para acelerar testes de vacinas contra Covid-19
Saúde e Ciência
Medida simplifica o procedimento, dispensando etapas, mas mantendo a exigência de requisitos técnicos essenciais do produto.
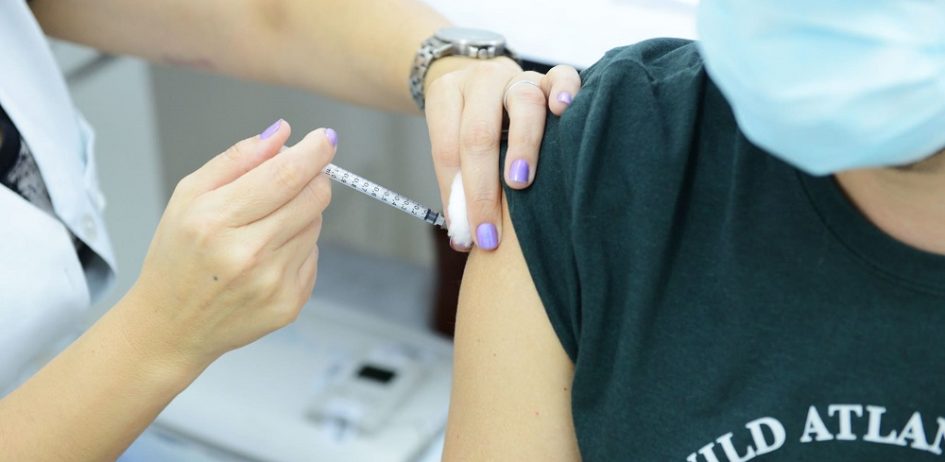
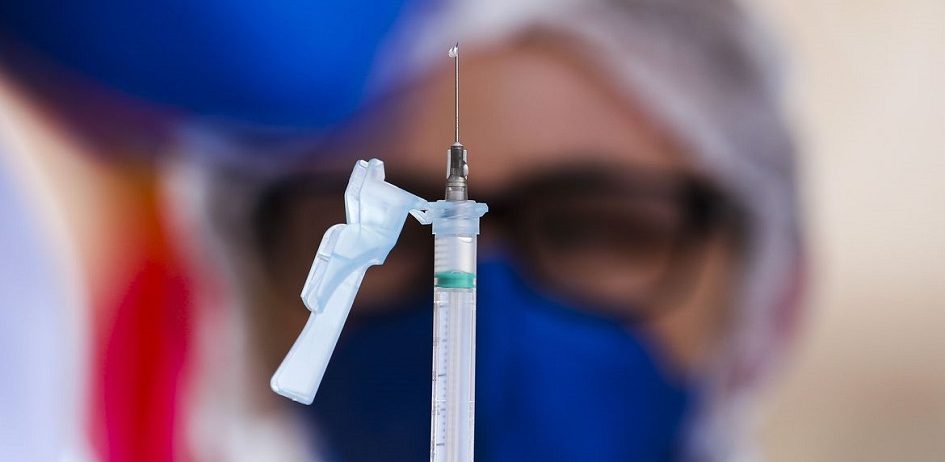
A Agência Nacional de Vigilância Sanitária – Anvisa aprovou um conjunto de regras que podem acelerar a distribuição de vacinas contra a Covid-19 à população brasileira. Trata-se da chamada “submissão contínua”, procedimento pelo qual os dados técnicos dos imunizantes deverão ser encaminhados à Agência conforme forem sendo gerados e não só ao final do processo. A medida simplifica o procedimento de registro dessas vacinas, dispensando etapas, mas mantendo a exigência de requisitos técnicos essenciais do produto, como “qualidade, segurança e eficácia”.
O gerente-geral de medicamentos e produtos biológicos da Anvisa, Gustavo Mendes, afirma não ser possível apontar qual será a redução do tempo de análise de empresas que seguirem a nova regra. “É preciso que as empresas se comprometam. Participem da submissão contínua”.
Mendes explica que a vantagem é permitir que a Anvisa antecipe a análise de partes dos estudos exigidos para o registro da vacina no país. A AstraZeneca e o Butantan usam este caminho para o desenvolvimento de imunizantes contra a covid-19. Os estudos pré-clínicos destes produtos, feitos em animais e laboratórios, já foram analisados pela Anvisa. Pela regra antiga, a Agência só avaliaria estes documentos no momento do pedido de registro da vacina, que ocorre após a finalização de estudos de “fase 3”, em humanos.
Na reunião da diretoria colegiada da Anvisa, os diretores dispensaram a realização de análise de impacto regulatório e de consulta pública da norma “devido ao grau de urgência e gravidade, caracterizadas por situação de iminente risco à saúde e necessidade de atuação imediata”. A nova instrução foi publicada no Diário Oficial da União – DOU de quarta-feira, 18.
Mendes afirma que o tempo médio de aprovação de registros de vacina pela Anvisa é de seis meses. Este período considera o tempo na fila par a análise, além da avaliação da Anvisa e questionamentos feitos às empresas. Mas há regra específica para produtos de combate à Covid-19, incluindo imunizantes, que obriga a agência a decidir em 60 dias. Além disso, estas vacinas serão priorizadas, ou seja, não enfrentaram as filas para entrar em análise.
De acordo com a decisão, o procedimento de “submissão contínua” será normatizado apenas para as vacinas contra covid-19 a serem registradas no País. “O que nós estamos propondo é uma forma exclusiva e diferenciada para tratar as vacinas referentes à covid-19. Isso precisa estar muito claro. Os demais produtos biológicos, novos ou não, seguirão o rito já vigente de submissão e análise”, explicou a diretora Alessandra Bastos Soares durante a reunião, conforme informações publicadas no site da agência.
A Anvisa destaca que outras autoridades regulatórias de referência, como a dos Estados Unidos, da Europa, da Suíça e da China, já utilizam a submissão contínua em situações específicas.
As empresas interessadas no procedimento simplificado de registro devem aderir ao modelo seguindo instruções descritas na IN. Para usufruto do procedimento diferenciado, a empresa deve atender a dois critérios: protocolar na agência dossiê de desenvolvimento clínico de medicamento referente à vacina proposta contra Covid-19 e estar com a vacina de interesse em fase 3 de desenvolvimento clínico.